2026年4月8日,由上海市东方医院(同济大学附属东方医院)牵头、多领域专家联合制定的《干细胞临床研究信息管理规范》(以下简称《规范》),正式刊载于《中国研究型医院(中英文)》2026 年第13卷第1期。这一权威标准的出台,为我国干细胞临床研究全流程信息管理提供了统一、可落地的技术指引,标志着行业从快速扩张正式迈入高质量、可追溯、安全可控的规范化发展新阶段。

长期以来,干细胞作为“活的药物”,其制备过程的复杂性、差异性一直是制约行业发展的痛点。过去我们主要依靠高等级实验室和熟练技术人员的“经验”来保障安全,而这部新规的落地,意味着行业正式转向依靠“制度”和“数据”来构建信任。在监管部门对“全过程追溯”要求日益严格的背景下,信息管理已不再是临床研究的“辅助项”,而是决定研究能否过关的“生死线”。
信息管理的核心:为细胞赋予合规身份
新规明确规定了干细胞临床研究中必要环节信息的管理要求,覆盖了从供者筛查、采集、制备、检验到放行、运输、使用、随访的全生命周期。其核心逻辑在于:只有记录清晰、数据完整的细胞,才是“合规”的细胞。
在信息管理的诸多环节中,制剂制备信息的管理尤为关键。干细胞制剂的生产过程极易受到环境波动、人为操作差异的影响。传统的人工培养模式下,记录往往滞后且存在主观性,一旦出现批次差异或不良事件,研究人员很难回溯是哪个环节出现了问题。

新规要求对制备过程进行详细记录,正是为了解决“追溯难”的问题。它要求每一份制剂都必须具备完整的“培养日志”,详细记录细胞的来源、传代时间、细胞密度、细胞形态等数十项信息。这不仅是对受试者负责,更是企业未来将技术从“研究”推向“药品”申报的必备证据。
技术赋能:全自动培养工作站助力临床项目实现信息规范记录
面对新规近乎严苛的记录要求,传统的人工手动记录已显得力不从心。在此背景下,友康生物通过自主研发的全自动细胞培养工作站,在兼具动态、全封闭、自动化培养的情况下,为行业提供了“合规于设计”的解决方案,帮助用户更便捷、更规范、更全面地记录制备信息。
全自动细胞培养工作站
高品质的细胞的低成本制备模式
二类医械,合规先行
该设备已获批北京市药监局第二类医疗器械注册证(注册证号:京械注准20252220109),为临床应用提供了合规保障。

01 [ 全封闭环境下的精准数据采集 ] .
友康全自动细胞培养工作站无需人工干预即可实时、自动记录温度、CO₂浓度及补液量、设备操作流程等关键参数。这种自动化记录彻底规避了人工记录可能存在的遗漏、篡改或滞后问题,完全符合新规对“及时性”和“准确性”的硬性要求。
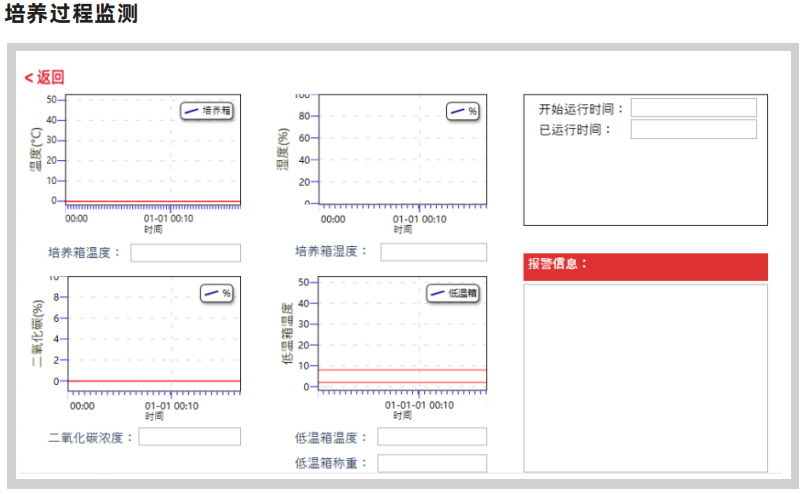
02 [杜绝交叉污染,确保数据纯净 ] .
信息管理的前提是样本安全。新规强调了对样本“身份识别”和防止混淆的要求。友康工作站采用的“一次性封闭管路系统”和“一机一样”的生产模式,使得每一次培养都是在独立的物理环境下进行。这不仅防止了生物学上的污染,更从物理上隔绝了信息记录张冠李戴的风险,确保了每一份细胞数据与细胞批次的唯一对应性。
03 [ 全流程追溯与审计追踪 ] .
对于监管机构而言,他们不仅关注细胞长得好不好,更关注“你怎么证明你养得好”。友康工作站能够导出全流程的操作日志和环境数据,形成符合GMP规范的审计追踪记录。这种“机器产出”的客观数据,比人工填写的表格更具法律效力和可信度。
YOCON
《干细胞临床研究信息管理规范》的发布,标志着中国干细胞行业正在经历一场深刻的供给侧改革。它正在将那些仅靠“手工作坊”模式、信息记录模糊的从业者挡在门外,而为那些拥抱自动化、数字化技术的企业铺平了道路。
在这个过程中,友康生物全自动细胞培养工作站不仅是提升效率的工具,更是满足合规要求、承载技术实力的载体。当每一份生物制剂都能拿出一份由机器生成、合乎规范、信息全面、无法篡改的“全周期培养记录”时,细胞治疗才能真正摆脱争议,走向标准化、规模化的商业成功。

 友康生物
友康生物 2026-04-28
2026-04-28 行业热点
行业热点



