2026年4月19日,国家卫健委科教司发布《关于生物医学新技术临床转化应用审批工作规范(征求意见稿)》(以下简称“征求意见稿”)。作为即将于2026年5月1日正式施行的《生物医学新技术临床研究和临床转化应用管理条例》(国务院令第818号)的关键配套文件,本次征求意见稿标志着我国细胞与基因治疗(CGT)产业在临床转化阶段迎来了更具操作性的监管框架。
本次征求意见稿释放了哪些关键监管信号?生物医学新技术的合规转化路径又将指向何方?本文将围绕上述问题,逐一进行梳理与探讨。
征求意见稿释放了哪些监管信号?
核心关键词解析
1 关键词一:审批范围
征求意见稿第三条明确,纳入审批范围的生物医学新技术需满足:(一)个性化程度高,国内尚无同类机制原理的药品获得上市许可或已启动确证性临床试验;(二)用于治疗《罕见病目录》收录的罕见病。

2 关键词二:多中心独立验证
征求意见稿第六条第(三)项明确要求,申请临床转化应用须具备“多中心独立验证一致”,即符合条件的其他医疗机构和卫生专业技术人员,遵守临床应用操作规范独立实施该技术,可以得到一致的安全性、有效性结论。

3 关键词三:安全性、有效性
征求意见稿第六条要求,临床研究须证明该技术“安全、有效”,符合伦理原则。第五条亦明确审批原则为“保证安全”。
4 关键词四:原材料与质量控制
征求意见稿第十一条、第十二条规定了材料核查程序,包括对技术成熟度、安全性、有效性、质量控制标准等的评估。

5 关键词五:全流程管理
征求意见稿第四章“临床应用管理”要求医疗机构建立生物医学新技术临床应用全流程管理制度,并定期上报应用情况和安全性数据。高风险技术批准后5年内、中风险3年内、低风险1年内仅限在原临床研究机构内开展。

合规之路该如何走?
友康生物合规性技术解决方案
为响应临床医院与生物制药企业的合规需求,友康生物聚焦细胞治疗产业链上游,提供覆盖从研发到生产全流程的完整工艺方案。我们深知,设备仅是技术载体,试剂仅为工艺环节中的单一组件。因此,我们的核心价值在于打通上下游环节,交付完整的技术解决方案,助力用户合规、高效地启动项目。

目前,全国已有多家三甲医院依托友康的合规方案开展细胞治疗新技术项目;超过40家药企采用友康产品进行细胞药物申报,并获得CDE受理;同时,我们与中国人民解放军总医院(301医院)共建的“骨类器官北京市重点实验室”,已成为产学研协同创新的重要范例。
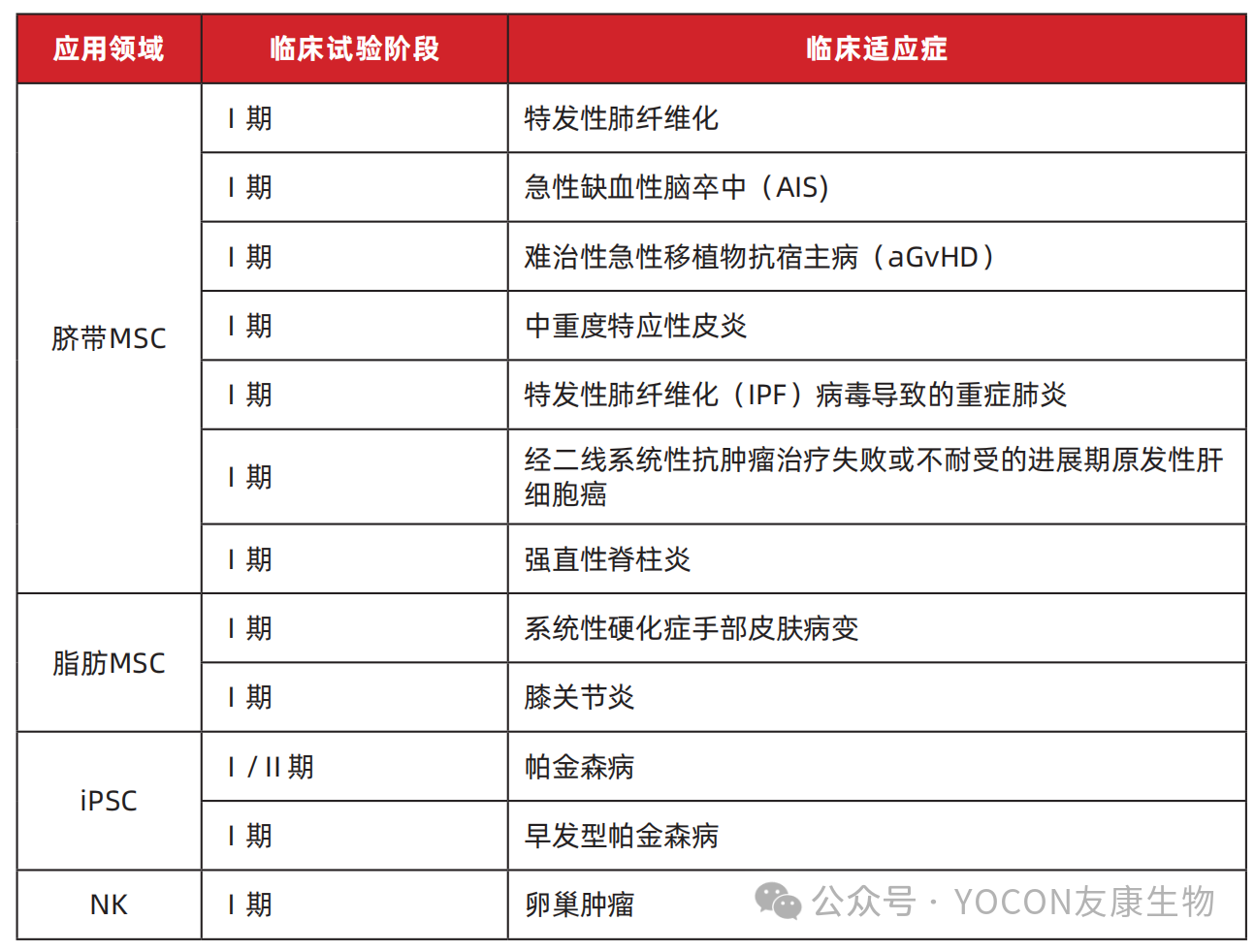

针对“安全性、有效性”原则:构建重组人血白蛋白体系
征求意见稿第十一条、第十二条要求对技术成熟度、安全性、有效性、质量控制标准进行评估。传统含血清或血浆来源白蛋白的培养基,存在病毒污染及批次间稳定性差的合规风险。
⚪友康方案:全面采用重组人白(rHSA)技术,NK细胞无血清培养基、T细胞无血清培养基、间充质干细胞无血清培养基等构建了完整的化学限定(CD)体系,从源头杜绝血源性传染病及异种蛋白免疫反应风险,完美契合审批对安全性的要求。

针对“多中心独立验证”原则:设备即工艺,实现多中心复制
征求意见稿第六条第(三)项要求“多中心独立验证一致”。对于细胞治疗这类“活的药物”,人工操作变异系数极高,难以满足不同中心间结果一致性的审查要求。
⚪友康方案:“设备是技术的载体,自动化是工艺的固化”。全自动细胞培养工站内部嵌套了经过验证的成熟细胞扩增工艺。无论在哪个实验室,只要启动工作站,输出的均是均一、高活率的细胞制剂,为多中心验证提供统计学上的工艺一致性保障。

针对“个性化程度高”原则:一次性封闭管路,杜绝交叉污染
征求意见稿第三条将“个性化程度高”作为审批范围的核心条件。自体细胞治疗要求严格的“一对一”独立培养,以保障样本的唯一性与安全性。
⚪友康方案:全自动工作站配套一次性封闭式FEP管路系统。每一例患者样本对应一套独立的培养管路套件;多模块工作站支持多个样本在同一个物理平台上独立运行,液路及控制系统完全隔离,符合防止交叉污染的核心要求。
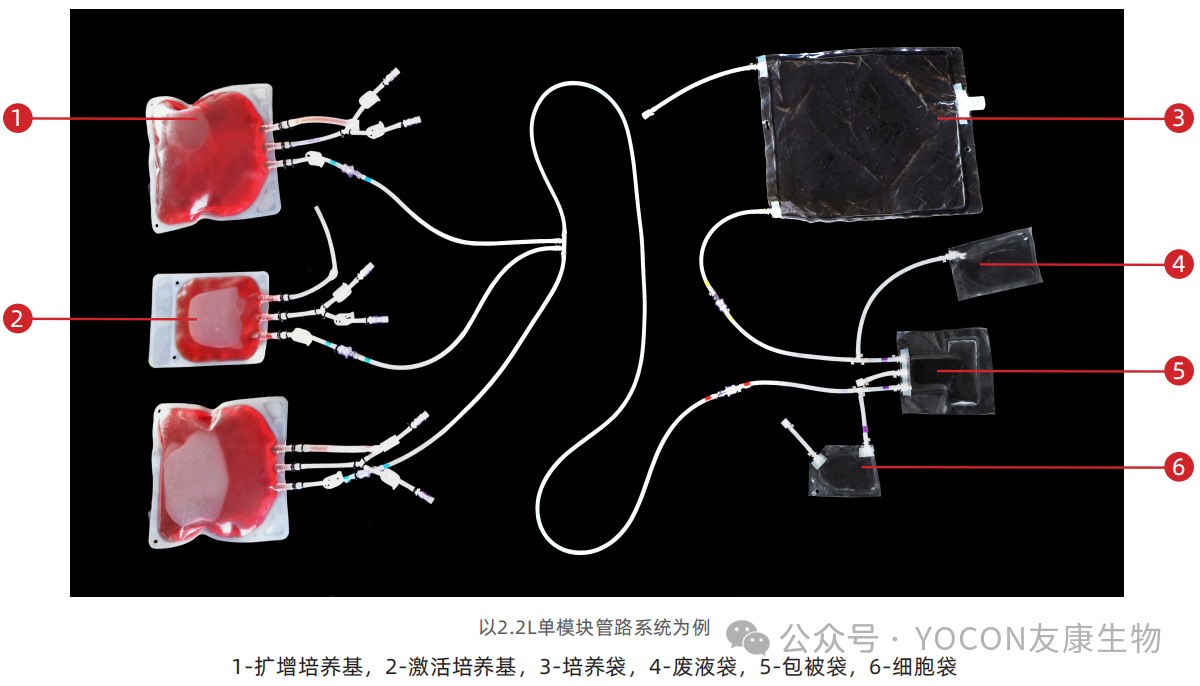
针对“全流程管理”原则:数据电子化管理
征求意见稿第四章要求医疗机构建立全流程管理制度,并定期上报应用情况和安全性数据。传统手工记录存在篡改风险和记录丢失隐患。
⚪友康方案:自动化工作站内置完整的电子批次记录,自动记录温度、pH、溶氧及培养过程操作,为审批提供不可篡改的原始数据支持。
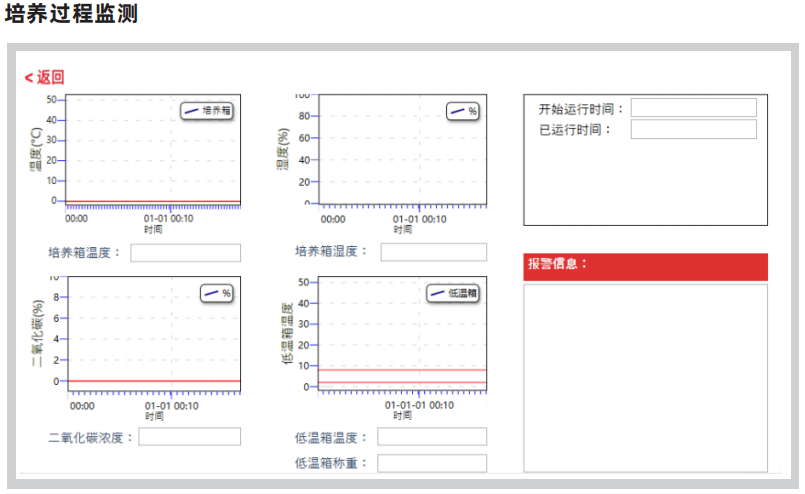
针对“材料核查与质量控制标准”原则:化学限定培养基保障可溯源性
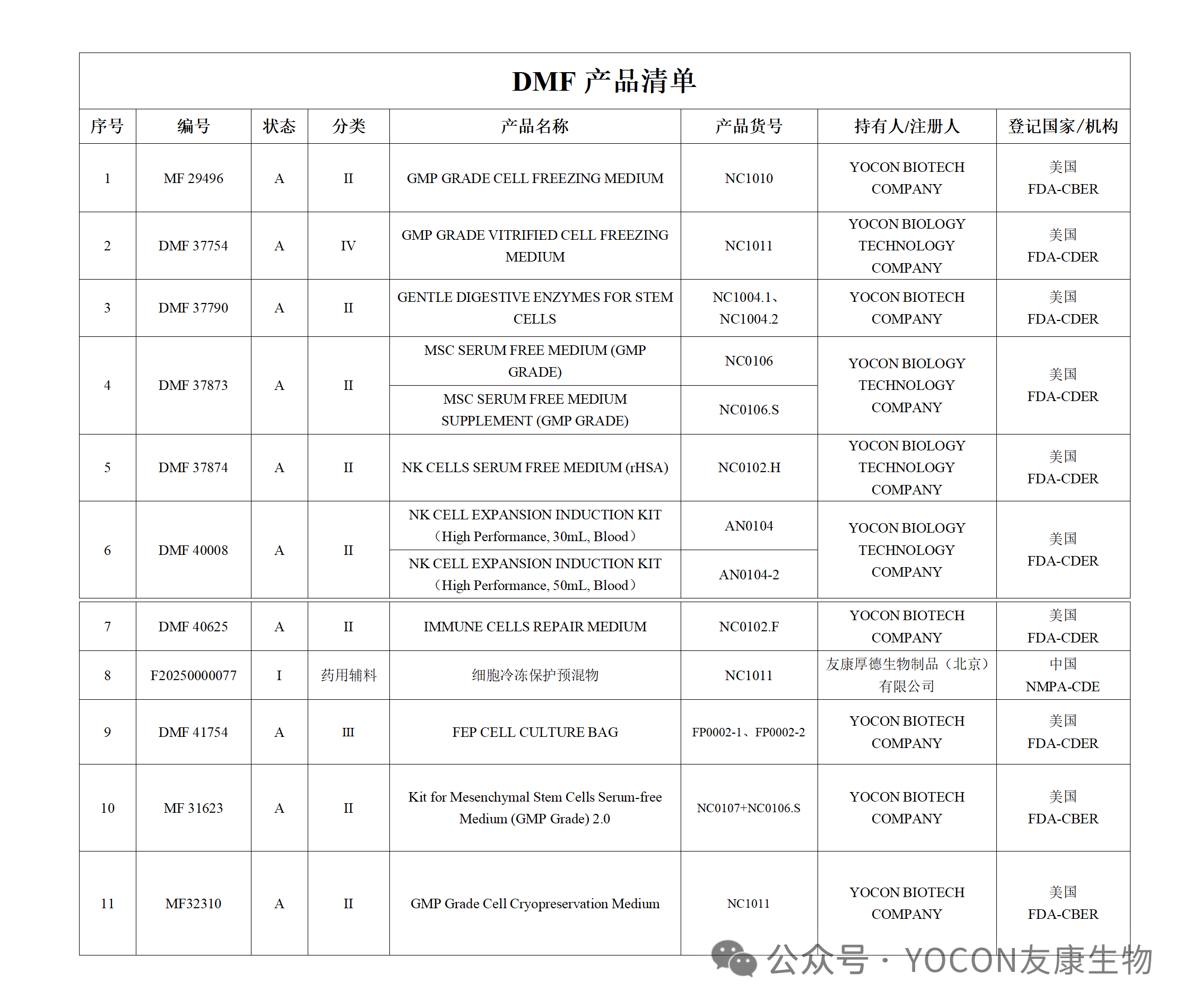
征求意见稿第十一条明确要求对质量控制标准进行评估。成分不明的培养基在材料核查中难以通过审评。
⚪友康方案:友康培养基坚持化学成分确定(CD)原则,每一种成分的分子结构和浓度都清晰明确,便于用户进行质量控制与溯源,是应对监管审查的最佳解决方案。
针对“风险分级管理”原则:自动化封闭系统降低技术风险
征求意见稿第十一条要求按照《生物医学新技术风险分级指南》划定技术的风险等级,高风险技术面临更严格的应用限制。
⚪友康方案:全封闭自动化培养系统大大降低了细胞制备过程中的污染风险和人为操作失误风险,有助于降低技术被划入高风险等级的可能性,或在高风险技术的严格监管下保障稳定的细胞制剂质量。

YOCON
2026年4月19日发布的《生物医学新技术临床转化应用审批工作规范(征求意见稿)》,通过“审批范围”“多中心独立验证”“安全性、有效性”“全流程管理”“伦理评估”等关键词,为行业描绘了清晰的监管路线图。“合规”不是天花板,而是入场券。以“化学成分确定的培养基”保障安全性,以“全自动封闭工作站”保障多中心一致性,不仅是技术供应的方向,更是行业应对新监管时代的必由之路。

 友康生物
友康生物 2026-04-27
2026-04-27 行业热点
行业热点



