近日,友康生物自主研发的GMP级间充质干细胞无血清培养基2.0(以下简称“GMP级培养基2.0”)正式通过美国FDA的DMF备案(备案号:31623)。这不仅意味着该产品可以支持中国药企用于中美联合细胞药物批准申请、药品注册,为全球细胞治疗产业提供强有力的工具支撑,也代表了友康在细胞培养试剂领域的技术实力得到了国际先进标准的认可。

突破技术壁垒,填补行业空白
间充质干细胞(MSCs)及其分泌的外泌体(MSC-EVs)是生命科学的“黄金资源”,前者因其强大的组织修复和免疫调节功能,在再生医学、抗衰老和疾病治疗中展现出无限应用前景;后者在药物递送、免疫调节和抗衰老中潜力巨大。
然而,当前市场上的培养基普遍存在两大短板:①功能单一:仅支持干细胞增殖,无法优化外泌体产量;②成分风险:含血清或不明添加物,导致外泌体纯化困难、临床应用安全性存疑。这一矛盾严重制约了间充质干细胞及其外泌体药物的规模化生产和标准化进程。
友康GMP级2.0培养基:一箭双雕的破局者
友康生物凭借多年技术积淀,推出的GMP级间充质干细胞无血清培养基2.0,可以实现“细胞高增殖+外泌体高收获”双重目标,其创新优势包括:

● 全新配方设计:在保障干细胞高活力扩增的同时,显著提升外泌体分泌量;
● 无动物源成分:化学成分明确,无人源动物源组分,杜绝外源性污染,培养基背景外泌体和不溶性颗粒物含量极低,外泌体更易纯化且符合FDA对细胞治疗产品的严格监管要求;
●支持大规模生产:适配细胞工厂、微载体、生物反应器等2D及3D大规模培养模式。
1、细胞传代性能
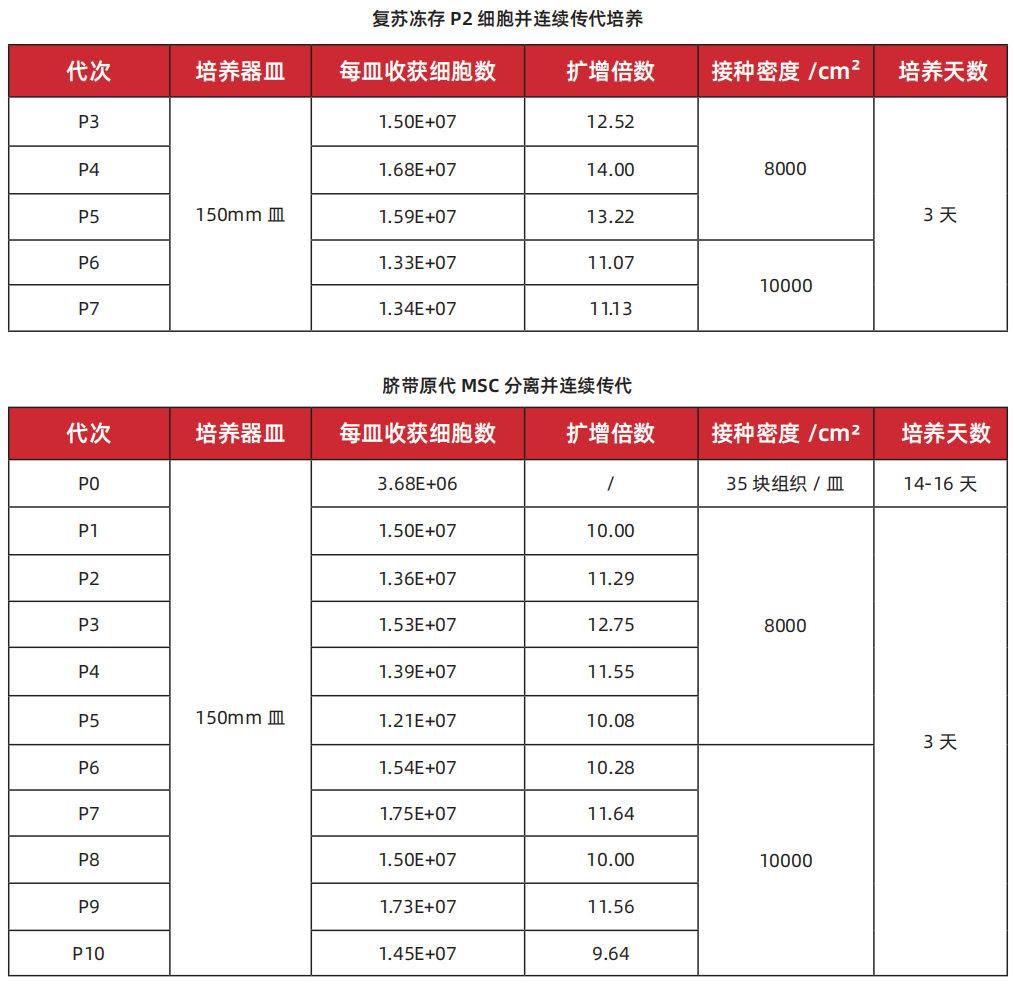
2、外泌体培养性能
①用于细胞工厂生产外泌体
复苏P2细胞,并连续传代至P3细胞时接种至细胞工厂,15天共收获外泌体2.52E+12个。
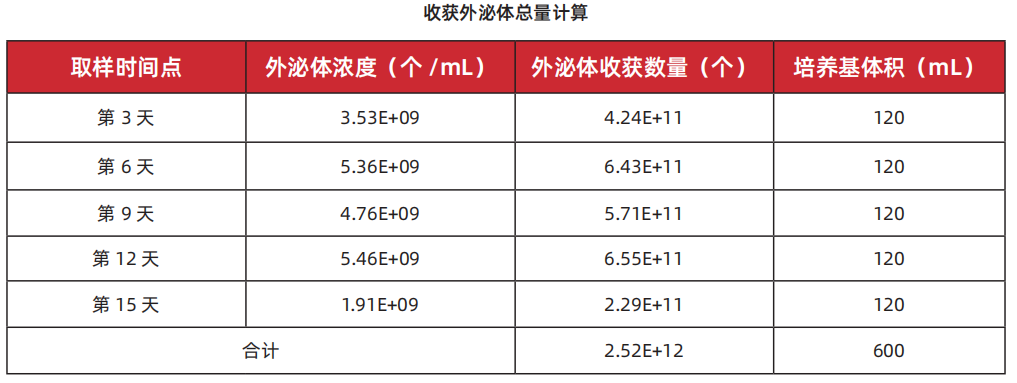
②用于微载体 3D 培养细胞收获外泌体
周期 15 天,500mL 培养基,共收获外泌体 3.50E+12 个。
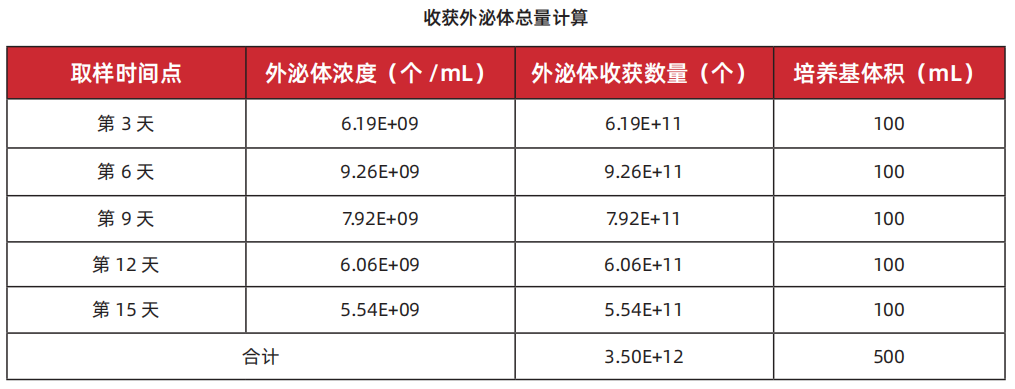
备案认证助力客户走得更远
美国FDA DMF备案是企业向FDA提交的保密技术档案,用于支持药物、生物制品或医疗器械的上市申请。此次备案成功,意味着友康培养基2.0的生产工艺、质量控制及安全性数据已获得FDA认可,未来可作为关键原料直接用于美国市场的细胞治疗产品申报,大幅降低下游药企的注册门槛与时间成本。
这一进展不仅为国内干细胞企业“出海”铺平道路,更将吸引国际药企与中国供应链合作,加速全球细胞治疗产业的商业化进程。
友康生物GMP级间充质干细胞无血清培养基2.0是友康多年技术攻坚的结果,为用户提供了“细胞培养+外泌体收获”双效解决方案。友康始终致力于为行业提供安全、可及的干细胞培养解决方案,助力细胞治疗从实验室走向临床。

 友康生物
友康生物 2025-06-17
2025-06-17 公司热点
公司热点



