嵌合抗原受体T细胞疗法(CAR-T)作为一种新型的精准靶向疗法,在21世纪彻底改变了癌症免疫治疗格局,已成为当今医学研究中最前沿热门的方向之一。CAR-T疗法通过基因工程改造患者自身的T细胞,使其能够精准识别并攻击癌细胞,尤其在白血病、淋巴瘤等血液肿瘤中展现出惊人的疗效,为越来越多的患者带来了希望以及生命质量的提升。
一、CAR - T细胞治疗的基本原理 CAR-T细胞疗法是一种高度个性化的肿瘤治疗手段。其核心在于通过基因工程技术,将能特异性识别肿瘤抗原的嵌合抗原受体(CAR)基因导入患者T细胞中,使其转化为CAR-T细胞。这些经过改造的T细胞,能够精准识别并高效杀伤表达特定抗原的肿瘤细胞,从而实现对肿瘤的靶向治疗。 CAR-T的生产制备流程主要包括最初分离和富集T细胞、T细胞活化、扩增、使用病毒或非病毒载体系统进行CAR基因转移、体外CAR-T细胞扩增,以及制成的细胞产品经过最后的末端工艺和冷冻保存等步骤。 二、慢病毒包装在CAR - T细胞制备中的关键作用 在CAR-T细胞的制备过程中,稳定转染是效应T细胞稳定表达CAR的前提。目前主流用于CAR-T的基因转导的方法仍是病毒转导,主要有γ-逆转录病毒和慢病毒。然而近年来,由于γ-逆转录病毒转导有引起插入致瘤的风险、不能感染非分裂细胞、病毒滴度低等问题,在临床试验中已经逐渐被慢病毒转导所取代。因此,慢病毒包装技术在CAR-T细胞制备中扮演着不可或缺的角色。 具体流程如下:首先,从患者外周血中分离出T细胞,并对其进行活化处理,使其处于易于接受外源基因的状态。随后,利用慢病毒载体将CAR基因导入T细胞内。由于慢病毒载体能够高效整合外源基因,确保了CAR基因在T细胞中的稳定表达,从而成功制备出CAR-T细胞。 那么,究竟什么是慢病毒载体呢? 三、慢病毒载体的特性与优势 慢病毒载体(Lentiviral vectors, LVs)起源于逆转录病毒科中的慢病毒属,其原型为人类免疫缺陷病毒(HIV)。为了使其能够安全应用于基因治疗,科学家对HIV-1基因组进行了改造。将HIV-1基因组分装于不同质粒,通过共转染细胞的方式,去除其自我复制能力,从而构建出仅具备单次感染能力的慢病毒载体。慢病毒载体基因组是单股正链RNA,其基因组进入细胞后,在细胞浆中被其自身携带的反转录酶反转为DNA,形成DNA整合前复合体,进入细胞核后,DNA整合到细胞基因组中。整合后的DNA转录成mRNA,回到细胞浆中,表达目的基因或片段。 目前广泛应用的四质粒系统,由包装质粒、包膜质粒、转移质粒以及辅助质粒构成,极大地提升了慢病毒载体的安全性与应用范围。其结构特点如下: - 包膜蛋白(如VSV-G):决定病毒感染范围和效率; - 基因组:携带目标基因(CAR序列)及必要包装元件(如LTR、Ψ包装信号); - 安全性改造:第三代慢病毒载体通过四质粒系统(转移质粒+包装质粒+包膜质粒+辅助质粒)剔除致病基因,确保无复制能力。 慢病毒载体的优势如下: - 高效转染:慢病毒载体可以感染分裂和非分裂细胞等多种细胞类型,对于原代细胞、干细胞以及不分化细胞等传统转染技术难以攻克的“堡垒”同样具有较高的转导效率。 - 持久表达:慢病毒载体独特的整合机制,能够将外源基因整合到宿主细胞的基因组中,实现基因的长期稳定表达。 - 容量大:慢病毒载体可以携带较大的基因片段,能够满足不同基因治疗的需求,尤其是针对复杂基因缺陷疾病的治疗中,具有不可替代的优势。 - 安全性高:经过改造的慢病毒载体不具有复制能力,不会导致病毒感染。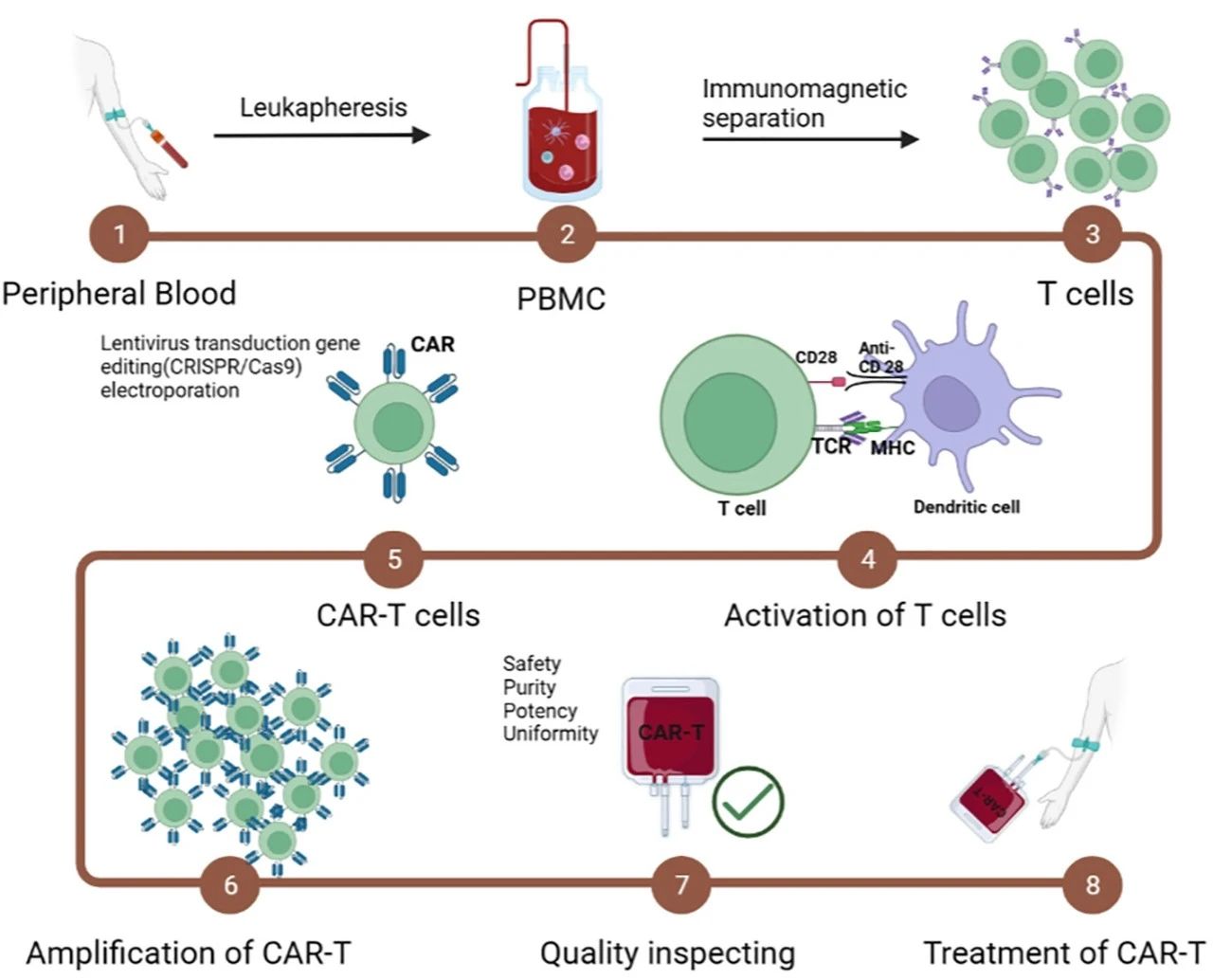
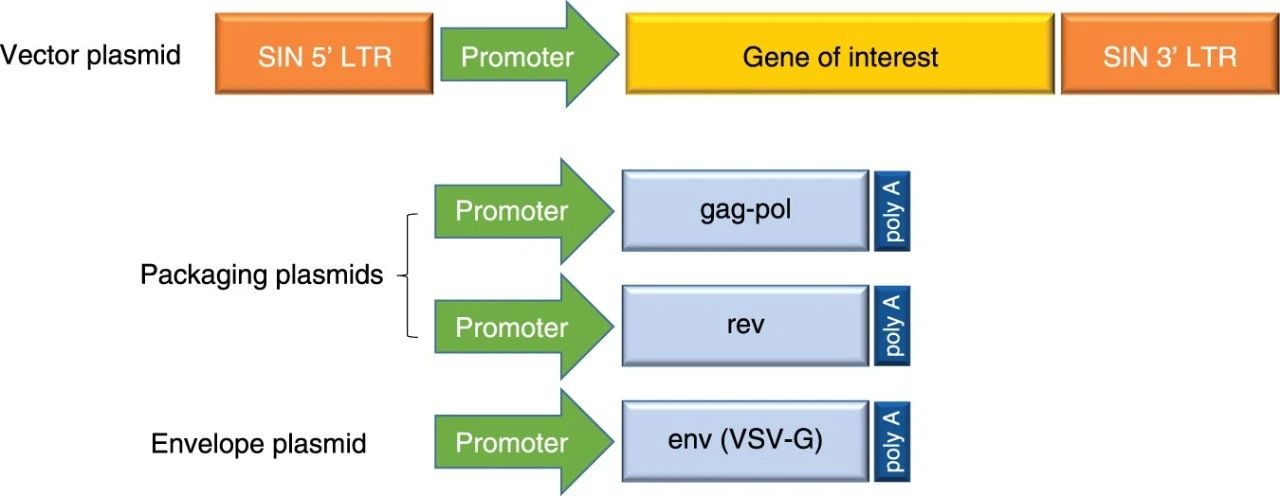
四、慢病毒载体的生产制备 慢病毒载体作为CAR-T的核心环节之一,其质量对细胞产品及其治疗效果具有直接影响。慢病毒载体的生产是一个复杂的过程,需要经过细胞培养、病毒包装和病毒纯化等多个步骤,其标准化流程包括: 1、细胞培养体系 - 细胞系的选择:大规模慢病毒生产通常选用HEK293T细胞系。该细胞系具有生长迅速、易于转染以及病毒产量高等显著优势,能够在悬浮培养条件下快速增殖,为慢病毒的大规模生产提供了理想的宿主细胞。 - 培养方式的演变:传统的贴壁培养方式在小规模研究中应用广泛,但在大规模生产中存在诸多局限性。随着技术的发展,悬浮无血清培养逐渐成为主流。由于化学成分明确且不含血清,这种培养方式不仅能有效降低生产成本和污染风险,还可以简化培养与后续纯化步骤,为慢病毒生产的规模化放大提供了有力支持。 2、病毒包装流程 - 质粒转染:当HEK293T细胞培养至合适密度时,将病毒包装质粒、包膜质粒以及携带CAR基因的转移质粒通过共转染的方式导入细胞内。转染过程中,各种质粒协同作用,启动慢病毒的包装程序。 - 病毒生产与收获:在转染后的数天培养过程中,HEK293T细胞会利用自身的生物合成机制,生产出大量慢病毒颗粒。这些颗粒释放至培养基中,通过离心、过滤等初步处理手段,即可收获含有慢病毒的上清液。 3、病毒纯化与质量控制 - 纯化方法:为了获取高纯度的慢病毒载体,常采用超速离心、离子交换层析(AEX)或亲和层析等技术手段,去除培养基中的杂质、细胞碎片以及未包装的质粒等成分,从而提高慢病毒载体的纯度与质量。 - 质量控制指标:慢病毒载体的质量控制涵盖多个方面,包括病毒滴度测定、纯度分析(检测宿主细胞蛋白、DNA残留量等)、活性评估(验证其对靶细胞的转导效率和CAR基因表达情况)以及安全性检测(如无菌检测、内毒素检测等),以确保慢病毒载体符合临床应用标准。 尽管慢病毒包装技术在CAR-T细胞治疗中取得了显著进展,但目前仍面临一些亟待解决的问题。一方面,慢病毒载体的理化性质相对不稳定,在储存和运输过程中容易发生降解,影响其转导效率和活性。另一方面,大规模生产过程中,慢病毒载体的回收率较低,生产成本居高不下,且培养体系和纯化工艺的优化仍存在较大空间,这些都限制了慢病毒包装技术的进一步推广应用。 慢病毒包装技术作为CAR-T细胞治疗的核心环节,在肿瘤免疫治疗领域发挥着至关重要的作用。深入研究慢病毒包装的生物学基础与生产工艺,克服当前面临的挑战,对于推动CAR-T细胞治疗技术的发展,乃至整个肿瘤免疫治疗领域的进步,都具有深远的意义。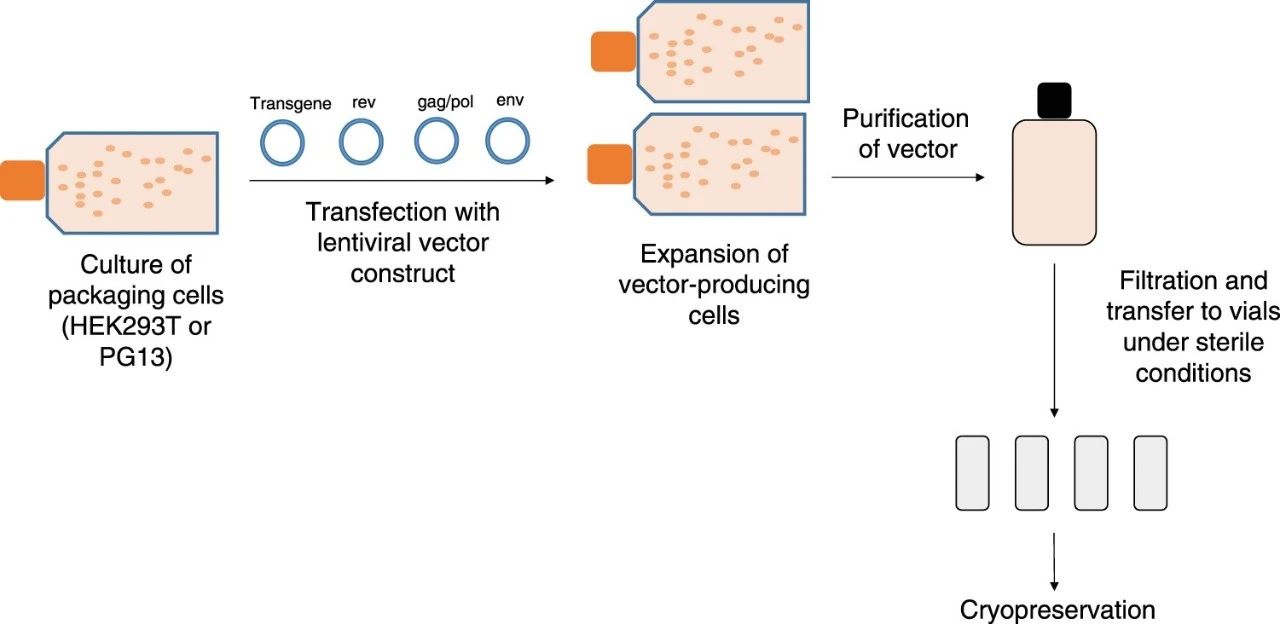

友康生物慢病毒包装上游培养工艺
友康生物提供悬浮HEK293慢病毒包装套装产品:包括HEK293全悬浮无血清培养基、无血清细胞冻存液、阳离子转染试剂以及HEK293细胞分散液等,助力实现高产量慢病毒载体生产。 货号 产品名称 产品用途 NC0303 HEK293全悬浮无血清培养基 该培养基用于悬浮HEK293细胞(如293T、293S、293E、293F)的连续培养以及外源基因的瞬时表达,高效表达外源蛋白,包装出的慢病毒滴度高。 NC1001 无血清细胞冻存液 支持高密度冻存间充质干细胞、免疫细胞、单个核细胞、杂交瘤等多细胞系。双重冷冻保护剂配方,细胞复苏活率与回收率稳定在90%以上。 AN105 阳离子转染试剂 本品用于外源基因的转染表达,搭配本公司HEK293全悬浮无血清培养基用于外源基因的高效表达。 NC1006 HEK293细胞分散液 本品用于悬浮HEK293细胞的精确计数,由于悬浮293细胞多以小团块状生长,需加入细胞分散液进行处理后才能较为准确的对之进行计数。 产品优势: 1、无血清,低蛋白,化学成分明确; 2、可扩展的悬浮培养体系; 3、操作简便,转染效率高; 4、病毒滴度 — 大于1.5e7 TU/mL 。 若对相关产品感兴趣,扫码联系友康生物

 友康生物
友康生物 2025-06-06
2025-06-06 公司热点
公司热点



